
3月赚140亿,这家中企被美国政府疯狂砸单的背后,3000亿新冠抗原检测市场结局难测
- 作者:飘飘
- 来源:健康界
- 发布时间:2022-05-12 15:08
3月赚140亿,这家中企被美国政府疯狂砸单的背后,3000亿新冠抗原检测市场结局难测
【概要描述】疫苗行业有目共睹,那新冠抗原检测市场究竟有多大?业界对此曾有诸多猜测。
- 作者:飘飘
- 来源:健康界
- 发布时间:2022-05-12 15:08
2022年4月,随着各家上市公司发布2021年年报,「全民免费的新冠疫苗有多赚钱?科兴盈利或超800亿」一度成为热搜。疫苗行业有目共睹,那新冠抗原检测市场究竟有多大?业界对此曾有诸多猜测。
例如,西南证券在研报中指出,新冠抗原家用自测试剂盒未来的主要市场预计来自美国、欧盟、日本以及中国,按照总人口和平均检测次数,预计全球市场潜力有望超过500亿美元(约合3168亿元人民币),其中美国市场占据大头,为79.2%,中国市场有望占16.8%。然而,疫情发展的不可预见性和防疫政策的不确定性,让这几千亿市场看起来颇为「朦胧」。企业到底能从中获得多少利润?行业是不是高估了这条赛道?众人存疑。
直至4月12日,九安医疗发布2022年第一季度业绩预告,预计一季度净利润为140亿元—160亿元,同比增长36707.43%—41965.63%。换算下来,相当于每一天赚1.56—1.78亿元。一时间,震惊业内,羡煞旁人。
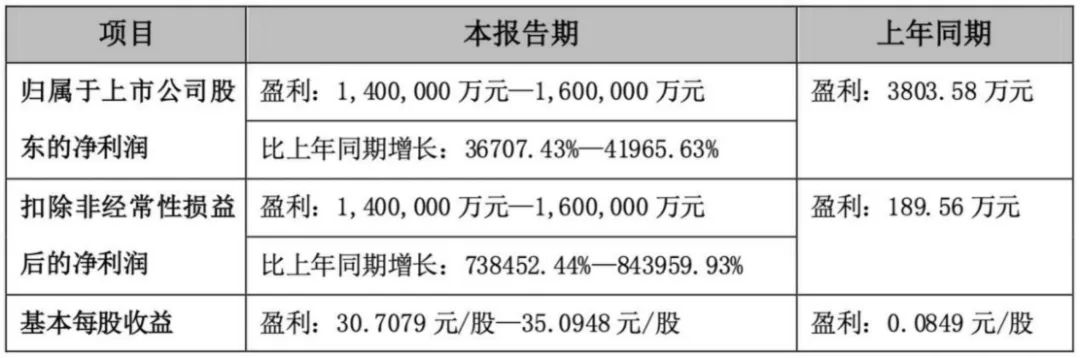
在公告中,九安医疗将业绩增长的原因归结为:受美国疫情发展的影响,当地对新冠抗原检测试剂盒产品需求大幅增长。
2022年1月份,九安医疗拿到美国 ACC(美国陆军合约管理指挥部)代表的美国HHS(美国卫生与公众服务部)的订单,向其销售总计3.54 亿人份的iHealth新冠抗原家用自测试剂盒产品,合同总金额达17.75亿美元,折算下来,每人份试剂盒单价约为5.01美元(约相当于32元人民币)。
如此看来,海外果然有「矿」,并且美国路线看起来,似乎比欧洲路线更赚钱。另一边,主攻国内抗原检测市场的企业面对的则是另一番光景:从集中获批,到史上最快集采,市场火速降温。
先入局者尚未吃到多少红利,家用新冠抗原检测试剂盒的价格便在短短几天内从20元-30元/人份下滑至不超过10元/人份。刨去成本,这个价格留给企业的利润空间已不多。
利润问题的核心,是受制于疫情的发展
故事还得从一支血压计讲起。2010年6月,九安医疗在深交所上市,成为国内血压计行业首家上市公司。上市后,九安医疗业绩平平。2013年至2019年,该公司扣非净利润连续7年亏损,到2019年,更是创下了亏损新高:亏损2.4亿元。直到疫情来了,凭借着额温计、血氧仪、制氧机等疫情物资,2020年,九安医疗终于迎来转机,当年扭亏为盈。营收为20.08亿元,大涨18436%;归母净利润2.42亿元,大涨264.68%。
2020年12月底的一天,九安医疗生化基础技术负责人齐艳玲收到了董事长刘毅的一条微信,是关于「厦门一家公司拿下了英国新冠检测试剂订单」,而且订单数额很大,又与九安公司业务非常近似。
刘毅表示:「出口欧洲市场已经是‘红海’了,而美国因为食品药品监督管理局(FDA)的门槛高,还是一片空白。」当时,美国真正的家庭试剂盒测试还没有开始。在重新审视后,公司下定决心,立项开始做试剂盒,向美国食品药品监督管理局发起冲击。2021年1月12日,九安医疗召开立项启动会。按照计划,九安医疗共制订了荧光试剂盒、机器识别方案等3个方案。经过多次尝试,原定的计划目标没有完成,海内外团队遭遇挫折。
经过每天国内外的团队视频进行沟通,盘点进度,近1年时间的艰苦努力,2021年11月8日,九安医疗宣布美国子公司的新冠抗原家用自测OTC试剂盒获得了美国食品药品监督管理局(FDA)的紧急使用授权(EUA),成为全球第一家以中国工厂申请获批的。
此后,九安医疗被美国政府、州政府疯狂砸单,自获批至今,九安医疗在美国共揽获合计21.08亿美元订单,折合人民币134.28亿元。九安医疗股价由此一路高涨,3个多月内斩获33个涨停板,市值一口气翻了12倍。
面对如雪花般的订单,九安医疗以天津为中心,与北京、河北唐山、河南郑州、山东潍坊等6个省、14个城市30多家外协工厂进行合作,从日产100万支、500万支、1000万支到2000余万支……
根据世界卫生组织最新发布的新冠肺炎每周流行病学报告,全球所有地区最近一周的新增病例数和死亡人数,均呈下降趋势。但报告同时提示,应谨慎看待这种下降趋势,因为部分国家正在逐步改变防控策略,导致进行的病毒检测减少。
浙商证券指出,很难认为奥密克戎会成为最后一个「超级变种」,预计抗疫将成为「持久战」。新冠检测产品作为抗疫全方位体系的第一道防线,预计其需求同样将常态化,后续的「超级变种」出现,将为其带来周期性。
哪些厂商又能够从中获益呢?浙商证券认为需要把握供需双方「六大要素」。
从需求方看:
第一是政策,例如获批厂家数量,政府免费发放带来采购大订单等;
第二是疫情严重程度,处于疫情爆发期的市场,更易发生医疗资源挤兑,带来更强烈的居家自检需求;
第三是支付能力,玩家会自发选择盈利性最好的市场。
从供给方看:
第一是海外渠道,有海外长期合作伙伴或海外子公司的企业往往能更快打入市场,提前获批;第二是产能,在当前仍有供需缺口情况下,产能较大的企业可以优先抢占市场及享受「红利期」;
第三是产品质量,疫情的严峻会对产品灵敏度、特异性提出越来越高的要求,而存在缺陷的产品,势必将提前退场。
欧洲:竞争格局呈恶化趋势
自2020年疫情爆发以来,核酸检测一直被视为新冠病毒检测的「金标准」。抗原检测相较起核酸检测,准确率略低,但胜在检测速度快、成本低。随着疫情的发展,2021年起,新冠抗原自测产品开始在欧洲主要国家大量使用。2021年2月,德国率先推行新冠抗原居家检测,并颁布相应自测准入资质。随后,法国比利时荷兰等国相继批准抗原自测产品。
中国是欧洲抗原检测试剂的主要供应国家之一。根据中国海关的统计数据,2021 年全年,中国抗原试剂盒合计出口金额约 714 亿元。浙江、福建和广东是主要的出口省份,进口国家主要是德国和英国。2022年1-2月,我国新冠试剂出口货值达到326亿元,且我国出口的新冠试剂,依然绝大部分为抗原检测试剂。
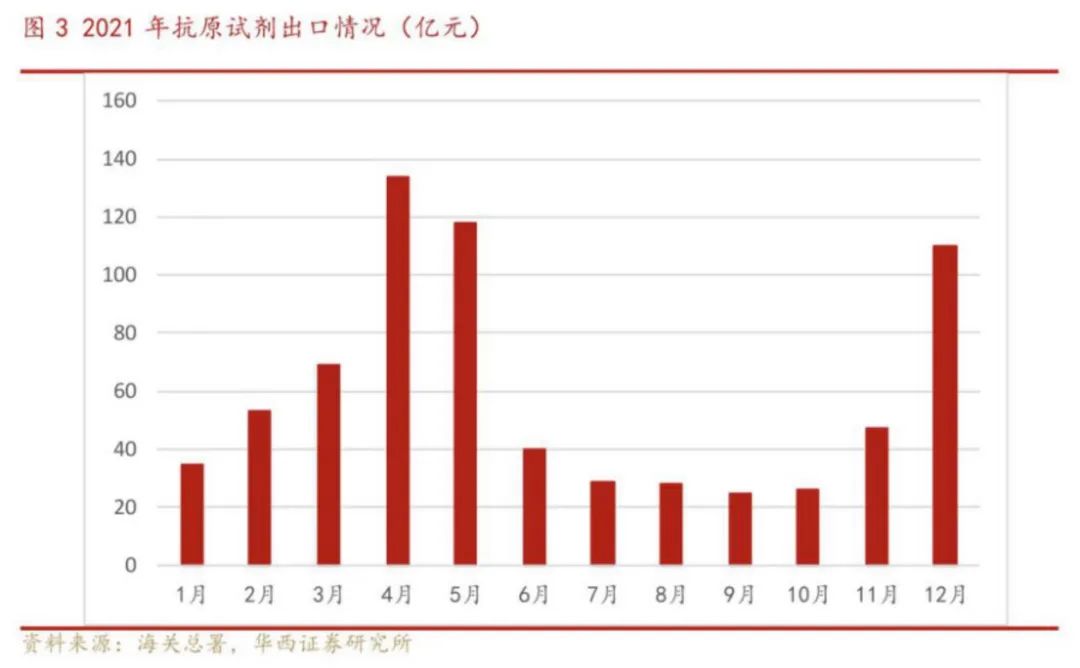
欧洲市场不算小,但落到单个企业上,能分得多少蛋糕?据西南证券统计,目前获得德国药监局(BfArM)批准的家用自测新冠抗原产品有43个,其中中国34个(企业30家)。另据广发证券研报,2021年第三季度后,欧盟开始收紧抗原自测产品的审批,由之前的各国自行紧急授权,改为由欧洲统一认证(CE),目前通过CE认证的抗原自测产品共616个,其中中国产品259种,涉及147家国内厂商。
入局者众多,市场竞争日渐激烈。从近期国内各新冠检测企业陆续公布的2021年业绩快报来看,主攻欧洲新冠抗原检测市场的企业,在2021年业绩皆有不同程度增长,但同时利润分化现象也很明显。
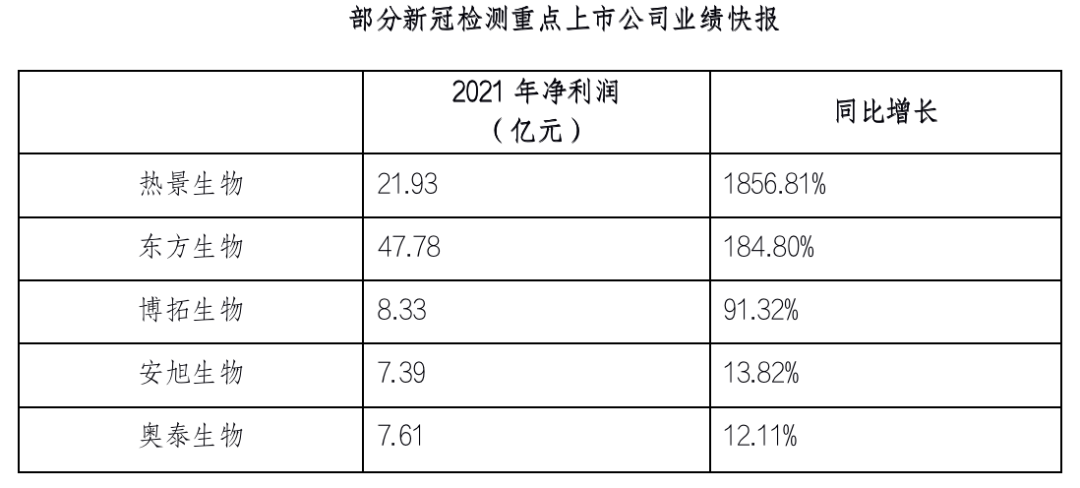
日前,荷兰、法国、德国等国宣布进一步放开新冠防疫措施,政府普遍不再强制居民做新冠病毒检测,仅对部分公共活动和社会场所有强制检测要求。新冠抗原检测以自我检测、自费购买为主。此外,新冠抗原自测产品价格较上市初期已大幅下降,终端价约为2-3欧元(相当于14到21元人民币)。
一位行业人士透露,欧洲各渠道1月份采购的抗原自测产品,截至3月还没有卖完,有不少货囤积在代理商手中。无论是需求端、供给端,抑或是价格端,欧洲抗原检测市场都显露出明显恶化迹象,前期的繁荣景象,恐难再现。
美国:竞争不激烈,利润空间较多
2021年2月,美国食品药品监督管理局批准了第一款居家检测的新冠抗原检测试剂,但直到2021年底,抗原自测产品才得到美国疾病控制与预防中心(CDC)的认可。
美国食品药品监督管理局对新冠抗原家用自测试剂的审批较为严格,目前仅批准了14个新冠抗原自测紧急使用授权(EUA)文号,涉及13家企业,其中国内厂家有3家:艾康生物、九安医疗、东方生物(西门子持证品牌商,东方生物为生产商)。
中航证券认为,新冠抗原检测的应用,有利于更及时发现无症状感染者,与当前的奥密克戎毒株及其变体的高传染性特征、疫情防控及时发现无症状感染者的需求非常匹配。随着奥密克戎的大流行,美国抗原自测产品需求迎来大规模增长,其中很大一部分采购需求来自于政府订单。
2022年1月4日,美国政府宣布将签署5亿份新冠检测采购合同;1月13日,美国政府宣布再追加采购5亿人份新冠检测试剂。首批采购,美国政府与雅培、罗氏和九安医疗一共签订了3.8 亿人份的合同,之后雅培与九安医疗又再获美国政府共计1.76亿人份的抗原检测试剂订单。西门子医疗也在1月份拿下了美国政府5000万个冠状病毒检测试剂盒的合同,这意味着其生产商东方生物有望因此获益。
1月15日起,美国政府要求保险公司必须报销非处方药(OTC)的新冠检测试剂盒,每人每月最多允许进行8次测试。东兴证券预测,按照美国 3.3 亿的人口推算,美国单月的新冠抗原检测的月度需求将超过20亿人份,其市场规模有望超过欧洲,预计后续美国市场还将继续新增订单。西南证券也认为,目前抗原自测产品在美国市场处于供不应求的状态,价格体系较好,并且预计未来较长时间,将维持较好的价格体系。
与此同时,包括美康生物、博拓生物、万孚生物在内的多家国内企业的试剂产品正在排队申请美国食品药品监督管理局的紧急授权。不过由于其审批很严,短期内美国市场的竞争格局依旧不激烈。
国内:集采冲击下,价格逐渐内卷
自2022年2月中旬以来,我国疫情开始呈现多点散发的趋势。3月11日,国务院新冠疫情联防联控组发布《关于印发新冠病毒抗原检测应用方案(试行)的通知》,正式提出在核酸检测基础上,增加抗原检测作为补充。
3月12日,国家药监局发布通告,批准5款新冠抗原产品自测应用申请变更。随后,新冠抗原检测试剂逐步进入各省集采范围,国家医保局也将新冠抗原检测纳入医保。
截至4月13日,国家药监局已批准27个新冠病毒抗原检测试剂产品。有业内人士表示,还有数十家企业正在排队入场拿证。但九安医疗仍然缺席。
新冠抗原检测最初的次均价格在 20-30 元之间,但随着生产批件的增加,以及集采的冲击,价格不断下滑。在广东集采中,万孚生物主动将价格从16.8元/人份降为9.8元/人份;在山东集采中,华大因源以7.9元/人份的价格中标;在陕西集采中,奥泰生物将40人份/盒的产品价格调整为6.5元/人份。目前,新冠抗原检测试剂盒最低价为5元/人份,来自山东博科诊断有限公司。
近期,上海疫情发展迅速,在核酸检测承压的情况下,上海市在全市范围内多次开展抗原检测。4月12日,上海市卫健委一级巡视员吴乾渝在发布会上透露,从4月11日开始,上海根据核酸筛查结果,划定了第一批封控区、管控区、防范区名单,实施分区分类差异化防控,防范区内人员落实一周2次抗原检测。
不止是上海,在香港、吉林新一轮的新冠疫情中,抗原检测作为核酸检测的补充手段,被应用于大规模筛查中。中航证券认为,由于生产门槛偏低和审批提速,新冠抗原检测试剂未来价格存在继续下降的可能,但由于消费频次较高,即使价格下降,业绩贡献还是可观的。
「利润问题的核心,是受制于疫情的发展,检测盒子是一种防疫物资,它一定是跟疫情变化起落的。」九安医疗创始人、董事长刘毅在接受媒体采访时直言。
责任编辑:亦欣
免责声明:仅用学习和交流,并不用于商业用途。图文著作权归原作者所有,在此向原作者表示感谢。除非无法确认,本网都会注明作者及来源。如有版权异义请及时告知。




















